Кардиальный механизм компенсации сердечной недостаточности
Original Medicine
Вирус иммунодефицита
 В 1982 году ученым удалось выяснить, что причиной СПИДа является вирус, который поражает клетки иммунной системы человека.
В 1982 году ученым удалось выяснить, что причиной СПИДа является вирус, который поражает клетки иммунной системы человека.
Табачная зависимость
 Только 5% курящих табак могут самостоятельно прекратить курение. 80% хотят прекратить курение табака, но им необходима медицинская помощь.
Только 5% курящих табак могут самостоятельно прекратить курение. 80% хотят прекратить курение табака, но им необходима медицинская помощь.
Формы перитонита
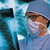 Перитонит — процесс воспаления брюшины, сопровождающийся тяжелым общим состоянием с симптомами нарушения функции жизненно важных органов.
Перитонит — процесс воспаления брюшины, сопровождающийся тяжелым общим состоянием с симптомами нарушения функции жизненно важных органов.
Уход за ребенком
 Уход является той основой, благодаря которой мы вправе рассчитывать на положительный эффект при организации лечения и воспитания детей.
Уход является той основой, благодаря которой мы вправе рассчитывать на положительный эффект при организации лечения и воспитания детей.
Этиология патологических болезней
Кардиальные механизмы компенсации сердечной недостаточности
Кардиальные адаптационно-компенсаторные механизмы имеют большое патогенетическое значение при хронической сердечной недостаточности. Под влиянием нейрогуморальных (нейрогормональных) воздействий, а также нередко вследствие влияния самого этиологического фактора (например, препятствия для выброса крови из левого желудочка при аортальном стенозе и т. д.) развивается концентрическая или эксцентрическая гипертрофия миокарда. Длительное существование увеличенной постнагрузки приводит к развитию концентрической гипертрофии миокарда — то есть к утолщению мышечной стенки без расширения полости желудочка. Увеличение толщины миокарда при концентрической гипертрофии позволяет развивать достаточное внутрижелудочковое давление в систолу и преодолеть значительно увеличенную постнагрузку и обеспечить адекватную перфузию органов и тканей. При увеличении преднагрузки постепенно развивается эксцентрическая гипертрофия, то есть умеренная гипертрофия миокарда, сопровождающаяся тоногенной дилатацией полости желудочка.
При миокардиальной недостаточности, то есть при хронической сердечной недостаточности, обусловленной поражением самого миокарда также развивается гипертрофия сердечной мышцы с тоногенной дилатацией левого желудочка различной степени выраженности.
Гипертрофия миокарда и умеренная тоногенная дилатация левого желудочка в течение определенного времени обеспечивают сохранение достаточной величины сердечного выброса, что происходит в соответствии с законом Старлинга. Как известно, имеется зависимость силы сокращения от исходной длины мышечного волокна, и эта зависимость является решающим фактором, определяющим функцию миокарда. Увеличение исходной длины мышечного волокна сопровождается возрастанием максимальной развиваемой силы сокращения (Braunwald и соавт., 1976). В соответствии с законом Стерлинга увеличение исходного конечного диастолического объема желудочка приводит к усилению его сокращения, что позволяет преодолеть увеличенную преднагрузку и постнагрузку.
Таким образом, с помощью гипертрофии миокарда, умеренной тоногенной дилатации желудочков и в соответствии с законом Стар-линга сердцу удается в течение определенного времени сохранять должную величину сердечного выброса и минутного объема и обеспечивать адекватное кровоснабжение органов и тканей. Однако с течением времени в условиях продолжающейся гемодинамической перегрузки или непосредственного повреждения миокарда компенсаторная реакция сердца становится недостаточной, эффективность механизма Стерлинга резко уменьшается при повышении конечного диастолического давления в левом желудочке выше 18— 20 мм рт. ст., сердечный выброс снижается. Уменьшение насосной функции сердца запускает процессы ремоделирования сердца, которые происходят под влиянием всех вышеуказанных патогенетических механизмов сердечной недостаточности, прежде всего высокой активности нейрогормональных систем, активности провос-палительных цитокинов, индукции апоптоза.
Согласно определению Pfeffer (1985), ремоделирование — это структурно-геометрические изменения левого желудочка, включающие в себя процессы гипертрофии миокарда и дилатации сердца, приводящие к изменению его геометрии и нарушению систолической и диастолической функции.
Основные компоненты ремоделирования левого желудочка представлены в табл. 40 и включают изменения на уровне отдельных кардиомиоцитов, изменения на уровне миокарда левого желудочка и изменения геометрии левого желудочка[2].
Механизм цианоза при сердечной недостаточности
Характерным признаком хронической сердечной недостаточности является цианоз кожи и видимых слизистых оболочек. Цианоз обусловлен снижением перфузии периферических тканей, замедлением в них кровотока, усиленной экстракцией кислорода тканями и увеличением вследствие этого концентрации восстановленного гемоглобина. Цианоз имеет характерные особенности, он наиболее выражен в области дистальных отделов конечностей (ладоней, стоп), губ, кончика носа, ушных раковин, подногтевых пространств (так называемый периферический, дистальный цианоз, или акроцианоз) и сопровождается похолоданием кожи конечностей (холодный цианоз). Акроцианоз часто сочетается с трофическими нарушениями кожи (сухость, шелушение) и ногтей (ломкость, тусклость ногтей).[3]
Использованные источники:
Кардиальные механизмы компенсации — сердечная недостаточность
Кардиальные адаптационно-компенсаторные механизмы имеют большое патогенетическое значение при хронической сердечной недостаточности. Под влиянием нейрогуморальных воздействий, а также нередко вследствие влияния самого этиологического фактора (например, препятствия для выброса крови из левого желудочка при аортальном стенозе и т. д.) развивается концентрическая или эксцентрическая гипертрофия миокарда. Длительное существование увеличенной постнагрузки приводит к развитию концентрической гипертрофии миокарда — то есть к утолщению мышечной стенки без расширения полости желудочка. Увеличение толщины миокарда при концентрической гипертрофии позволяет развивать достаточное внутрижелудочковое давление в систолу и преодолеть значительно увеличенную постнагрузку и обеспечить адекватную перфузию органов и тканей. При увеличении преднагрузки постепенно развивается эксцентрическая гипертрофия, то есть умеренная гипертрофия миокарда, сопровождающаяся тоногенной дилатацией полости желудочка.
Гипертрофия миокарда и умеренная тоногенная дилатация ЛЖ в течение определенного времени обеспечивают сохранение достаточной величины сердечного выброса, что происходит в соответствии с законом Стерлинга — увеличение исходного конечного диастолического объема желудочка приводит к усилению его сокращения, что позволяет преодолеть увеличенную преднагрузку и постнагрузку.
Однако с течением времени в условиях продолжающейся гемодинамической
перегрузки или непосредственного повреждения миокарда компенсаторная реакция сердца становится недостаточной, эффективность механизма Стерлинга резко уменьшается, сердечный выброс снижается. Уменьшение насосной функции сердца запускает процессы ремоделирования сердца, которые происходят под влиянием всех вышеуказанных патогенетических механизмов сердечной недостаточности, прежде всего, высокой активности нейрогуморальных систем.
Ремоделирование — это структурно-геометрические изменения ЛЖ, включающие в себя процессы гипертрофии миокарда и дилатации сердца, приводящие к изменению его геометрии и нарушению систолической и диастолической функции.
- -Изменения на уровне отдельных кардиомиоцитов:
— нарушение образования АТФ в процессе окислительного фосфорилирования и истощение запасов АТФ и креатинфосфата,
— экспрессия фетальной формы тяжелой цепи головки миозина с низкой АТФазной активностью,
— нарушение структуры и экспрессии белков, обеспечивающих сопряжение возбуждения и сокращения,
— десентизация b-адренорецепторного аппарата кардиомиоцитов,
— гипертрофия,
— нарушение функции белков цитоскелета.
2. Изменение миокарда ЛЖ:
— уменьшение количества кардиомиоцитов (за счет некроза и апоптоза),
— изменения во внеклеточном матриксе (активация металлопротеиназ, деградация матрикса, замещающий фиброз).
3. Изменения геометрии ЛЖ:
— дилатация,
— сферическая конфигурация,
— истончение стенки,
— функциональная (относительная) митральная регургитация.
В основе приблизительно 25-30% всех случаев хронической сердечной недостаточности лежит диастолическая дисфункция ЛЖ, то есть невозможность миокарда полностью расслабиться в момент диастолы и вместить требуемый объем крови.
Установлено, что по мере усугубления миокардиальной дисфункции уменьшается плотность на мембране саркоплазматического ретикулума молекул Са++- АТФазы (этот феномен может обнаруживаться уже на стадии компенсаторной гипертрофии миокарда) и компенсаторно (для предупреждения перегрузки цитоплазмы кардиомиоцитов ионами кальция) повышается активность Na+/Ca++-обменника. Способность кардиомиоцитов снижать внутриклеточный уровень ионов Са++ во время релаксации до исходного и насыщать ионами кальция саркоплазматический ретикулум прогрессивно падает, что связано с падением в кардиомиоцитах концентрации АТФ и снижением соотношения АТФ/АДФ («энергетическое голодание»).
Скорость расслабления миокарда в диастолу определяется также аффинностью тропонина С к ионам Са++ и АТФазной активностью головок миозина. Аффинность тропонина С к ионам Са++ при хронической сердечной недостаточности может оказаться повышенной, что приведет к значительному затруднению высвобождения и удаления Са++ из цитозоля кардиомиоцита, что соответственно замедляет релаксацию миокарда. В последние годы установлена огромная роль избыточного накопления коллагена в интерстициальном пространстве в повышении жесткости миокарда и, следовательно, в нарушении его способности расслабляться в диастоле. До тех пор, пока гипертрофия миокарда сопровождается пропорциональным увеличением как мышечного, так и сосудистого и интерстициального компонентов миокарда, она носит адаптивный характер и является концентрической. Когда же начинает избыточно развиваться соединительная ткань и преобладать периваскулярный и интерстициальный фиброз, гипертрофия миокарда становится патологической, эксцентрической и со временем приводит вначале к диастолической, а затем и к систолической дисфункции сердца.
Клиническая картина
Среди всех случаев хронической сердечной недостаточности около 70—75% приходится на долю систолической формы. При ишемической болезни сердца, артериальной гипертензии, дилатационной кардиомиопатии, некоторых ревматических пороках сердца (например, аортальных) вначале развивается клиническая симптоматика хронической левожелудочковой недостаточности (ЛЖСН), в последующей по мере прогрессирования основного заболевания и продолжающегося снижения сократительной функции миокарда ЛЖ развиваются легочная гипертензия и правожелудочковая недостаточность, таким образом, хроническая сердечная недостаточность становится бивентрикулярной (БЗСН).
Далее излагается клиническая симптоматика хронической БЗСН. В конце раздела будут выделены клинические особенности ЛЖСН и правожелудочковой сердечной недостаточности (ПЖСН).
Использованные источники:
МЕХАНИЗМЫ КОМПЕНСАЦИИ ПРИ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Механизмы компенсации при сердечной недостаточности делятся на две группы:
1. Интракардиальные (миокардиальные):
Срочные интракардиальные механизмы:
1) в ответ на кратковременную перегрузку объемом — гетерометрический механизм компенсации (закон Франка-Старлинга);
2) в ответ на кратковременную перегрузку давлением — гомеометрический механизм компенсации (феномен Анрепа);
3) рефлекс Бейнбриджа;
4) в ответ на острое повреждение и гибель части кардиомиоцитов — заместительный склероз (замещается только дефект структуры, функция не компенсируется).
Долговременные интракардиальные механизмы — это прогрессирующий процесс ремоделирования миокарда, зависящий от пускового фактора и представленный в виде компенсаторной гиперфункции сердца, в основе которой лежит гипертрофия миокарда.
Экстракардиальные механизмы компенсации при сердечной недостаточности:
I. Компенсаторная гиперактивация нейрогуморалъных систем, направленная на повышение работы сердца:
1) симпатоадреналовой системы (САС);
2) миокардиальной ренин-ангиотензиновой системы (РАС);
3) системы ренин-ангиотензин-альдостерон-АДГ (РААС-АДГ).
II. Компенсаторная гиперактивация дублирующих кислородтранспортных систем — эритропоэза и внешнего дыхания.
Проявления этой группы механизмов: вторичный эритроцитоз с повышением вязкости крови и повышением нагрузки на сердце; одышка.
Гетерометрический механизм (закон Франка-Старлинга) — это такой механизм компенсации, возникающий при перегрузке объемом, в основе которого лежит увеличение напряжения и силы сердечных сокращений в от-
вет на увеличение растяжения миокарда под влиянием избыточного объема крови.
Гомеометрический механизм (феномен Анрепа) — это такой механизм компенсации, возникающий при повышении сопротивления оттоку крови, в основе которого лежит постепенное повышение силы сердечных сокращений без значительного изменения длины мышечных волокон. В этом случае длина мышечного волокна практически не увеличивается (поэтому и механизм называется гомеометрическим), но повышается давление и напряжение, возникающее при сокращении мышц в конце диастолы. Повышение силы сердечных сокращений происходит не сразу, а постепенно, пока не достигнет уровня, необходимого для сохранения минутного объема крови. Этот механизм развивается при стенозах клапанов сердца, артериальной гипертензии и др. Из двух описанных механизмов наиболее полезен гетерометрический механизм, так как меньше потребляется кислорода, меньше расходуется энергии.
Рефлекс Бейнбриджа — это развитие тахикардии (увеличение частоты сердечных сокращений) вследствие повышения давления крови в полных венах, правом предсердии и растяжения их.
Использованные источники:
Сердечная недостаточность (сн)
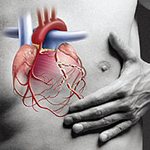
Сердечная недостаточность кровообращения – типовая форма патологии сердца, при которой нагрузка, падающая на сердце, превышает его способность совершать адекватную потребностям организма работу.
По характеру течения различают острую и хроническую сердечную недостаточность. По локализации сердечная недостаточность может быть левожелудочковой, правожелудочковой и тотальной, когда имеются признаки нарушения работы обоих желудочков. По механизму развития различают первичную (кардиальную) сердечную недостаточность, когда понижается насосная функция сердца и вторичную (некардиальную) гиподиастолическую, когда снижается диастолическое наполнение полостей сердца (например, при скоплении жидкости полости перикарда).
Различают три патофизиологических варианта развития кардиальной сердечной недостаточности (СН):
1. Миокардиальная СН возникающая в результате повреждения миокарда (физические факторы – травма, действие электротока; химические факторы – катехоламины, тироксин, дефицит кислорода, субстратов окисления, витаминов; биологические факторы – инфекции, токсины, паразиты.
2. Сердечная недостаточность, вызванная перегрузкой миокарда увеличенным объемом крови или давлением.
3. Смешанная сердечная недостаточность, когда поражение миокарда и повышенная нагрузка на сердце действуют одновременно (пример эндомиокардит).
Патогенез развития сердечной недостаточности. Механизмы компенсации сердечной недостаточности.
К снижению сократительной способности миокарда и развитию СН приводят:
1. Нарушение энергообеспечения миокарда из-за дефицита кислорода и субстратов окисления
2. Повреждение мембран и ферментных систем кардиомиоцитов: детергентное действие накапливающихся НЭСК (неэстерифицированные жирные кислоты), разрушение кардиомиоцитов гидролазами лизосом, повреждение мембран и ферментов свободными радикалами и продуктами перекисного окисления липидов.
3. Нарушение трансмембранного распределения и транспорта ионов и воды – дисиония и гипергидратация.
Снижение сократительной способности миокарда и развитие СН приводит к включению кардиальных и экстракардиальных механизмов компенсации.
Кардиальные механизмы компенсации сердечной недостаточности:
1. Гетерометрический механизм Франка – Старлинга – усиление сердечных сокращений в ответ на увеличение диастолического наполнения полостей сердца и увеличения длины мышечных волокон (тоногенная дилятация миокарда).
2. Гомеометрический механизм – усиление сердечных сокращений в ответ на повышенное сопротивление сердечному выбросу крови, возникающему при стенозе отверстий или повышении артериального давления.
3. Увеличение частоты сердечных сокращений – тахикардия.
4. Усиление симпатоадреналовых влияний на сердце – увеличение концентрации катехоламинов в миокарде и усиление их захвата кардиомиоцитами.
Все это экстренные механизмы компенсации СН. Далее включается долговременный механизм компенсации СН – гипертрофия миокарда – увеличение массы миокарда за счет увеличения каждого отдельного мышечного волокна, но не их числа.
Различают три стадии гипертрофии:
1. Аварийная стадия. Увеличение нагрузки на сердце вызывает увеличения функционирования каждого отдельного мышечного волокна. Увеличивается отношение работы к массе миокарда — увеличение интенсивности функционирования структур (ИФС). ИФС вызывает обменные нарушения – распад АТФ увеличении концентрации АДФ и неорганического фосфора (НФ) усиление гликолиза, ацидоз, усиление биосинтетических процессов (увеличения числа митохондрий, миофибрил) и постепенное увеличение массы миокарда.
2. Стадия завершившейся гипертрофии и устойчивой гиперфункции. Постепенное увеличение массы миокарда приводит к нормализации соотношения работы к массе, к нормализации ИФС и восстановлению обмена веществ в миокарде.
3. Длительная гипертрофия приводит к развитию третьей стадии — прогрессирующего кардиосклероза. Развитие этой стадии обусловлено постепенным ухудшением питания, гибелью кардиомиоцитов и замещением их соединительной тканью, так как гипертрофия сосудов и нервов отстает от гипертрофии мышечных волокон.
Постепенно прогрессирующий кардиосклероз приводит к развитию СН.
Гипертрофия сердца, возникающая у спортсменов, называется физиологической в отличие от патологической гипертрофии у больных.
Отличие физиологической гипертрофии от патологической:
1. При физиологической гипертрофии у спортсмена периоды интенсивной нагрузки сменяется периодами отдыха. В периоды отдыха сердце полностью восстанавливает свои энергетические пластические и регуляторные ресурсы. У больного нагрузка носит, как правило, постоянный характер, и сердце не восстанавливается.
2. Физиологическая гипертрофия гармонична – наблюдается равномерная гипертрофия всех отделов сердца. При патологической гипертрофии увеличивается один из отделов сердца, а другие либо не изменяются, либо могут даже атрофироваться. Так, при стенозе митрального отверстия, вся нагрузка падает на левое предсердие, а в левый желудочек поступает меньшее, чем в норме количество крови.
3. При физиологической гипертрофии миокарда увеличивается функциональная приспособляемость сердца. Функциональная приспособляемость сердца – это способность сердца менять объем своей работы от максимума до минимума в соответствии с потребностями организма. У спортсменов минимум уменьшается (брадикардия) максимум увеличивается. При патологической гипертрофии минимум увеличивается, а максимум уменьшается, и функциональные возможности тоже уменьшаются.
4. У спортсменов наблюдается увеличение массы скелетной мускулатуры и массы сердечной мышцы. При работе скелетных мышц вырабатывается молочная кислота, которая может использоваться сердечной мышцей. При патологической гипертрофии сердца масса сердечной мышцы растет, а скелетная мускулатура атрофируется.
При недостаточности сердца в организме развивается кислородное голодание тканей (гипоксия). В ответ на гипоксию возникают экстракардиальные механизмы компенсации сердечной недостаточности:
Спазм периферических сосудов, выброс крови из кровяных депо и увеличение массы циркулирующей крови; эритроцитоз, увеличение содержания гемоглобина в крови и увеличение кислородной емкости крови; усиление работы системы дыхания; усиление гликолиза в тканях.
Наряду с развитием механизмов компенсации у больных наблюдаются гемодинамические и клинические признаки декомпенсации сердечной недостаточности.
Гемодинамические признаки сердечной недостаточности:
1. Падение минутного объема сердца – уменьшение количества крови выбрасываемой сердцем в аорту за 1 минуту.
2. Неполное опорожнение желудочков приводит к увеличению остаточного систолического объема – увеличение количества крови оставшейся в полостях сердца после его систолы.
3. Повышение кровенаполнения полостей сердца ведет к повышению диастолического давления и к миогенной дилятяции (расширение полостей сердца) миокарда.
4. Повышение давления на путях притока и снижение давления на путях оттока крови – повышение венозного и снижение артериального давления крови.
Основными клиническими проявлениями сердечной недостаточности являются одышка, цианоз, отеки.
Использованные источники:
