Патогенез тахикардии при сердечной недостаточности
Аритмия сердца. Сердечная недостаточность
Аритмия сердца – это нарушения периодичности возбуждения и сокращения сердца, его ритмичности.
Аритмия, болезнь широко распространённая, она может возникнуть во время любого сердечного заболевания и под воздействием вегетативного, эндокринного и прочих метаболических нарушений. Серьёзное значение имеют электролитные расстройства, а именно, отклонения от нормы калия и кальция, содержащихся в клетке. Аритмия может возникнуть при интоксикации организма и при некоторых действиях лекарства, она может быть связана с врождёнными особенностями проводящей системы.
В основе аритмии лежит нарушение электрофизиологических качеств проводящей системы и сократительного миокарда. Диагностируют аритмии, как правило, по ЭКГ, в виде: синусовой аритмии, пароксизмальной тахикардии, экстрасистолии, трепетания предсердий, мерцания предсердий, трепетания и мерцания желудочков, атриовентрикулярной блокады, синоатриальной блокады, блокады ножек пучка Гисса и т.д.
Сердечная недостаточность
Это недостаточность кровообращения. Хронической сердечной недостаточностью называют состояние, при котором сердце не может справиться со своими насосными функциями, то есть, оно не обеспечивает нормального кровообращения. Причин появлению такого состояния довольно много: это и ишемическая болезнь сердца, и его пороки, и артериальная гипертензия, а также диффузные заболевания лёгких, дистрофия миокарда, миокардит и пр.
Симптомы и течение хронической сердечной недостаточности.
Симптомы различают в зависимости от поражённого отдела сердца. Так, при недостаточности работы левого желудочка у больного появляется одышка, при сидении наблюдается упор рук в колени, в целом сердцебиение учащенное. Параллельно может наблюдаться проявление недостаточности мозгового кровообращения – головокружения, потемнение в глазах и даже обмороки. Недостаточность работы правого желудочка сердца проявляется в набухании вен шеи, синюшностью кончиков пальцев, губ и носа, увеличением печени, различными отёками тела и полостей организма. При длительном течении сердечной недостаточности кожа больного становится тонкой, дряблой, она блестит, отёки покрывают все тело, происходит постепенное истощение организма.
Нормальный ритм сердцебиения обеспечивается автоматически синусовым узлом, он так и называется — синусовый. Частота синусового ритма у большинства взрослых здоровых людей, находящихся в состоянии покоя, составляет 60-75 ударов в минуту.
Синусовая аритмия
Синусовая аритмия – это синусовый ритм, при котором превышена разница между интервалами R-R на ЭКГ на 0,1 с. Дыхательная синусовая аритмия – это физиологичное явление, которое более заметно у молодых людей и при медленном глубоком дыхании по пульсу или ЭКГ. Среди факторов, учащающих синусовый ритм, можно отметить физические и эмоциональные нагрузки, симпатомиметики. Они способны уменьшить или полностью устранить дыхательную синусовую аритмию. Синусовая аритмия, которая не связанна с дыханием, встречается крайне редко. Сама по себе она лечения не требует.
Синусовая тахикардия
Временные проявления синусовой тахикардии возникают под влиянием симпатомиметиков, атропина, при быстром снижении артериального давления любого происхождения, после приёма алкогольных напитков. Стойкая синусовая тахикардия возникает во время лихорадки, тиреотоксикоза, миокардита, при сердечной недостаточности, проявлении анемии и тромбоэмболии легочной артерии. Она может сопровождаться ощущением собственного сердцебиения.
Лечение аритмии и сердечной недостаточности должно быть направлено на устранение основного заболевания. При проявлении тахикардии, которая обусловлена тиреотоксикозом, вспомогательное значение имеет использование бета-адреноблокаторов. Синусовая тахикардия, связанная с нейроциркуляторной дистонией, лечится применением в малых дозах седативных средств и бета-адреноблокаторами. При тахикардии, обусловленной сердечной недостаточностью, врач назначает сердечные гликозиды.
Использованные источники:
Наджелудочковая тахикардия
Наджелудочковая (суправентрикулярная) тахикардия – это повышение частоты сердечных сокращений более 120-150 ударов в минуту, при котором источником сердечного ритма служит не синусовый узел, а любой другой участок миокарда, располагающийся выше желудочков. Среди всех пароксизмальных тахикардий такой вариант аритмии наиболее благоприятный.
Приступ наджелудочковой тахикардии обычно не превышает нескольких суток и часто купируется самостоятельно. Постоянная наджелудочковая форма встречается крайне редко, поэтому правильнее такую патологию расценивать в качестве пароксизма.
Классификация
Наджелудочковая тахикардия в зависимости от источника ритма делится на предсердную и предсердно-желудочковую (атриовентрикулярную) формы. Во втором случае регулярные нервные импульсы, распространяющиеся по всему сердцу, генерируются в предсердно-желудочковом узле.
Согласно международной классификации выделяют тахикардии с узким комплексом QRS и широким QRS. Наджелудочковые формы делятся на 2 вида по такому же принципу.
Узкий QRS-комплекс на ЭКГ формируется при нормальном прохождении нервного импульса от предсердия к желудочкам через атриовентрикулярный (АВ) узел. Все тахикардии с широким QRS подразумевают возникновение и функционирование патологического предсердно-желудочкового очага проведения. Нервный сигнал проходит минуя АВ-соединение. Из-за расширенного QRS-комплекса такие аритмии на электрокардиограмме довольно тяжело отличить от желудочкового ритма с увеличенной частотой сердечных сокращений (ЧСС), поэтому купирование приступа проводится точно так же, как при желудочковой тахикардии.
Распространенность патологии
Согласно мировым наблюдениям, наджелудочковая тахикардия встречается у 0,2-0,3 % населения. Женщины в два раза чаще страдают этой патологией.
В 80 % случаев пароксизмы возникают у людей старше 60-65 лет. У 20 человек из ста заболевших диагностируются предсердные формы. Остальные 80 % страдают предсердно-желудочковыми пароксизмальными тахикардиями.
Причины наджелудочковой тахикардии
Ведущими этиологическими факторами патологии выступают органические повреждения миокарда. К ним относятся различные склеротические, воспалительные и дистрофические изменения ткани. Данные состояния чаще возникают при хронической ишемической болезни сердца (ИБС), некоторых пороках и иных кардиопатиях.
Развитие суправентрикулярной тахикардии возможно при наличии аномальных путей проведения нервного сигнала к желудочкам от предсердий (к примеру, WPW-синдром).
По всей вероятности, несмотря на отрицания многих авторов, существуют нейрогенные формы пароксизмальной наджелудочковой тахикардии. Такая форма нарушения ритма может возникнуть при повышенной активации симпатической нервной системы во время избыточной психоэмоциональной нагрузки.
Механические воздействия на сердечную мышцу в некоторых случаях также являются виновниками возникновения тахиаритмий. Это встречается при наличии в полостях сердца спаек или дополнительных хорд.
В молодом возрасте часто невозможно определение причины наджелудочковых пароксизмов. Вероятно, это связано с изменениями в сердечной мышце, которые не изучены, либо не определены инструментальными методами исследования. Однако, такие случаи расцениваются как идиопатические (эссенциальные) тахикардии.
В редких случаях основной причиной наджелудочковой тахикардии является тиреотоксикоз (реакция организма на повышенный уровень гормонов щитовидной железы). Ввиду того, что это заболевание может создать некоторые препятствия в назначении противоаритмического лечения, анализ на гормоны необходимо выполнить в любом случае.
Механизм возникновения тахикардий
В основе патогенеза наджелудочковой тахикардии лежит изменение структурных элементов миокарда и активация пусковых факторов. К последним относятся нарушения электролитного состава, изменение растяжимости миокарда, ишемия и действие некоторых лекарственных препаратов.
Ведущие механизмы развития пароксизмальных наджелудочковых тахикардий:
- Повышение автоматизма отдельных клеток, расположенных на всем пути проводящей системы сердца с триггерным механизмом. Такой вариант патогенеза встречается редко.
- Механизм re-entry. В этом случае происходит круговое распространение волны возбуждения с повторным входом (основной механизм развития наджелудочковой тахикардии).
Два вышеописанных механизма могут существовать при нарушении электрической однородности (гомогенности) мышечных клеток сердца и клеток проводящей системы. В подавляющем большинстве случаев межпредсердный пучок Бахмана и элементы АВ-узла способствуют возникновению аномального проведения нервного импульса. Гетерогенность вышеописанных клеток обусловлена генетически и объясняется различием работы ионных каналов.
Клинические проявления и возможные осложнения
Субъективные ощущения человека с наджелудочковой тахикардией весьма разнообразны и зависят от степени выраженности заболевания. При частоте сердечных сокращений до 130 — 140 ударов в минуту и короткой продолжительности приступа пациенты могут вообще не ощущать никаких нарушений и не знать о пароксизме. Если ЧСС достигает 180-200 ударов в минуту, больные в основном жалуются на тошноту, головокружение или общую слабость. В отличие от синусовой тахикардии, при данной патологии вегетативные симптомы в виде озноба или потливости выражены в меньшей степени.
Все клинические проявления напрямую зависят от вида суправентрикулярной тахикардии, реакции организма на нее и сопутствующих заболеваний (особенно болезни сердца). Однако, общим симптомом практически всех пароксизмальных наджелудочковых тахикардий является ощущение учащенного или усиленного сердцебиения.
Возможные клинические проявления у больных с поражением сердечно-сосудистой системы:
- обмороки (примерно в 15 % случаев);
- боли в области сердца (чаще у больных с ИБС);
- одышка и острая недостаточность кровообращения со всевозможными осложнениями;
- сердечно сосудистая недостаточность (при длительном течении приступа);
- кардиогенный шок (в случае возникновения пароксизма на фоне инфаркта миокарда или застойной кардиомиопатии).
Пароксизмальная наджелудочковая тахикардия может проявляться абсолютно по-разному даже у людей одного и того же возраста, пола и состояния здоровья организма. У одного больного кратковременные приступы случаются ежемесячно/ежегодно. Другой же пациент может лишь единожды в жизни перенести длительный пароксизмальный приступ без вреда для здоровья. Существует много промежуточных вариантов заболевания относительно вышеописанных примеров.
Диагностика
Заподозрить у себя такое заболевание должен человек, у которого без особых на то причин резко начинается и точно так же резко заканчивается либо ощущение учащенного сердцебиения, либо приступы головокружения или одышки. Для подтверждения диагноза достаточно изучить жалобы пациента, выслушать работу сердца и снять ЭКГ.
При выслушивании работы сердца обычным фонендоскопом можно определить ритмичное учащенное сердцебиение. При ЧСС, превышающей 150 ударов в минуту, сразу же исключается вариант синусовой тахикардии. Если же частота сокращений сердца более 200 ударов, то и желудочковая тахикардия также маловероятна. Но таких данных недостаточно, т.к. в вышеописанный диапазон ЧСС может входить и трепетание предсердий, и правильная форма мерцательной аритмии.
Косвенными признаками наджелудочковой тахикардии являются:
- частый слабый пульс, неподдающийся точному подсчету;
- снижение артериального давления;
- затрудненное дыхание.
Основу диагностики всех пароксизмальных наджелудочковых тахикардий составляет ЭКГ-исследование и Холтеровское мониторирование. Иногда приходится прибегать к таким методам, как ЧПСС (чреспищеводная стимуляция сердца) и нагрузочные ЭКГ-пробы. Реже, при крайней необходимости, проводят ЭФИ (внутрисердечное электрофизиологическое исследование).
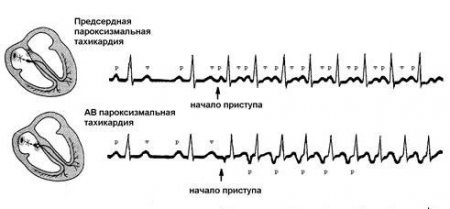 Результаты ЭКГ исследования при разных видах наджелудочковой тахикардии Основными признаками наджелудочковой тахикардии на ЭКГ является повышение ЧСС больше нормы с отсутствием зубцов P. Иногда зубцы могут быть двухфазными или деформированными, однако, из-за частых желудочковых QRS-комплексов их обнаружить не удается.
Результаты ЭКГ исследования при разных видах наджелудочковой тахикардии Основными признаками наджелудочковой тахикардии на ЭКГ является повышение ЧСС больше нормы с отсутствием зубцов P. Иногда зубцы могут быть двухфазными или деформированными, однако, из-за частых желудочковых QRS-комплексов их обнаружить не удается.
Существует 3 основные патологии, с которыми важно провести дифференциальную диагностику классической наджелудочковой аритмии:
- Синдром слабости синусового узла (СССУ). В случае не обнаружения существующего заболевания купирование и дальнейшее лечение пароксизмальной тахикардии может быть опасным.
- Желудочковая тахикардия (при ней желудочковые комплексы очень похожи на таковые при QRS-расширенной наджелудочковой тахикардии).
- Синдромы предвозбуждения желудочков. (в т.ч. WPW-синдром).
Лечение наджелудочковой тахикардии
Лечение полностью зависит от формы тахикардии, длительности приступов, их частоты, осложнений заболевания и сопутствующей патологии. Наджелудочковый пароксизм должен быть купирован на месте. Для этого обязателен вызов скорой медицинской помощи. При отсутствии эффекта или развитии осложнений в виде сердечно-сосудистой недостаточности или острого нарушения сердечного кровообращения показана срочная госпитализация.
Направление на стационарное лечение в плановом порядке получают пациенты с часто рецидивирующими пароксизмами. Таким больным проводится углубленное обследование и решение вопроса о хирургическом лечении.
Купирование пароксизма наджелудочковой тахикардии
При данном варианте тахикардии достаточно эффективны вагусные пробы:
- проба Вальсальвы — натуживание с одновременной задержкой дыхания (самая эффективная);
- проба Ашнера – надавливание на глазные яблоки в течение короткого промежутка времени, не превышающего 5-10 секунд;
- массаж каротидного синуса (область сонной артерии на шее);
- опускание лица в холодную воду;
- глубокое дыхание;
- приседание на корточки.
Эти способы купирования приступа нужно применять с осторожностью, т.к. при перенесенном инсульте, тяжелой форме сердечной недостаточности, глаукоме или СССУ данные манипуляции могут нанести вред здоровью.
Часто вышеописанные действия неэффективны, поэтому приходиться прибегать к восстановлению нормального сердцебиения при помощи лекарственных препаратов, электроимпульсной терапии (ЭИТ) или чреспищеводной стимуляции сердца. Последний вариант применяют при непереносимости антиаритмических препаратов или при тахикардии с водителем ритма из АВ-соединения.
Для правильного выбора способа лечения желательно определить конкретную форму наджелудочковой тахикардии. В связи с тем, что на практике довольно часто существует экстренная необходимость в купировании приступа «сию минуту» и нет времени для дифдиагностики, ритм восстанавливается согласно алгоритмам, разработанным Министерством Здравоохранения.
Для предупреждения рецидивов пароксизмальной суправентрикулярной тахикардии применяют сердечные гликозиды и антиаритмические препараты. Дозировку подбирают индивидуально. Нередко в качестве противорецидивного препарата применяют то же лекарственное вещество, которым удачно купировался пароксизм.
Основу лечения составляют бета-блокаторы. К ним относятся: анаприлин, метопролол, бисопролол, атенолол. Для лучшего эффекта и с целью снижения дозировки эти лекарственные вещества используют совместно с антиаритмическими препаратами. Исключение составляет верапамил (данный препарат высокоэффективен для купирования пароксизмов, однако, его необоснованное сочетание с вышеописанными препаратами крайне опасно).
С осторожностью нужно подходить и к лечению тахикардии при наличии WPW-синдрома. В этом случае в большинстве вариантов также запрещено применять верапамил, а сердечные гликозиды стоит использовать с особой осторожностью.
Помимо этого, доказана эффективность и других противоаритмических препаратов, которые назначают последовательно в зависимости от тяжести и купируемости пароксизмов:
- соталол,
- пропафенон,
- этацизин,
- дизопирамид,
- хинидин,
- амиодарон,
- новокаинамид.
Параллельно приему противорецидивных препаратов исключается применение любых лекарственных веществ, способных вызвать тахикардию. Нежелательно также употреблять крепкий чай, кофе, алкоголь.
В тяжелых случаях и при частых рецидивах показано хирургическое лечение. Существует два подхода:
- Разрушение дополнительных проводящих путей химическим, электрическим, лазерным или другим способом.
- Имплантация кардиостимуляторов или мини-дефибрилляторов.
Прогноз
При эссенциальной пароксизмальной наджелудочковой тахикардии прогноз чаще благоприятный, хотя полное излечение случается довольно редко. Суправентрикулярные тахикардии, возникающие на фоне сердечной патологии, более опасны для организма. При правильном лечении высока вероятность его эффективности. Полное излечение также невозможно.
Профилактика
Специфического предупреждения возникновения наджелудочковой тахикардии не существует. Первичная профилактика – недопущение основного заболевания, вызывающего пароксизмы. К вторичной профилактике можно отнести адекватную терапию патологии, провоцирующей приступы наджелудочковой тахикардии.
Таким образом, наджелудочковая тахикардия в большинстве случаев представляет собой неотложное состояние, при котором требуется экстренная помощь медицинских специалистов.
Использованные источники:
Патогенез тахикардии при сердечной недостаточности
Нарушение диастолического расслабления миокарда
Функциональная перегрузка миокарда может быть вызвана чрезмерным увеличением количества притекающей к сердцу крови (преднагрузка), либо сопротивления, которое развивается при изгнании крови из желудочков в аорту и легочный ствол (постнагрузка). В таких случаях говорят о систолической форме сердечной недостаточности. Возможно развитие диастолической формы сердечной недостаточности, характеризующейся нарушениями расслабления миокарда и увеличением ригидности стенок желудочков. Формирование обеих форм наблюдается в результате следующих изменений.
I. В самом сердце: (1) пороки клапанов сердца, (2) уменьшение массы сократительного миокарда (инфаркт и т.п.), (3) кардиосклероз.
II. В сосудистом русле: (1) артериальная гипертензия, (2) артериовенозные шунты.
III. В системе крови: (1) гиперволемия, (2) полицитемия.
IV. В системе нейрогуморальной регуляции деятельности сердца: (1) чрезмерное влияние на миокард симпатоадреналовой, ангиотензиновой систем, (2) тироксина, (3) предсердного натрийуретического фактора.
Согласно современным представлениям, выделяют три патофизиологических варианта сердечной недостаточности:
Сердечная недостаточность от перегрузки (перегрузочная);
2) Сердечная недостаточность вследствие заболеваний самого миокарда (миокардитическая);
3) Смешанная форма сердечной недостаточности (сочетания перегрузочной и миокардиальной).
Помимо этих форм сердечной недостаточности, которые условно можно назвать первичными, или кардиогенными, встречаются и такие, которые обусловлены первичным уменьшением притока крови к сердцу. Их обозначают как вторичные, или некардиогенные. Они могут быть результатом значительного снижения массы циркулирующей крови, нарушения диастолического расслабления миокарда при его сдавлении жидкостью, накапливающейся в полости перикарда (экссудат, кровь), и других подобных состояниях. Подчеркнем, что ведущими причинами сердечной недостаточности (70-80%) являются ИБС, гипертоническая болезнь и их сочетание, а также пороки сердца (10-15%).
По преимущественно пораженному отделу сердца выделяют: (1) левожелудочковую, (2) правожелудочковую, (3) тотальную формы.
По скорости развития выделяют (1) острую (минуты, часы, дни) и (2) хроническую (недели, месяцы, годы) сердечную недостаточность.
Гемодинамические показатели при хронической недостаточности изменяются следующим образом:
1. МОС снижается с 5,5 до 3,5 л/мин., реже – не изменяется или повышается (например, при гиперволемии);
2. Время кругооборота в системном кровотоке увеличивается с 20-23 до 90 и более секунд (в малом круге кровообращения до 10-12 сек.).
3. Объем циркулирующей крови возрастает;
4. АД практически не меняется;
5. Венозное давление повышается (растет давление наполнения, расширяются капилляры, посткапилляры, венулы, давление крови в них повышается);
6. Конечнодиастолическое давление в желудочках повышается;
7. Конечнодиастолический объем крови в желудочках увеличивается.
Патогенез сердечной недостаточности. Сердечная недостаточность как вследствие перегрузки сердца давлением и объемом крови (перегрузочная форма), так и вследствие прямого поражения миокарда (миокардиальная форма), проявляется снижением его сократительной функции. Ограничение насосной функции запускает кардиальные и экстракардиальные компенсаторные механизмы. Условно выделяют пять кардиальных механизма адаптации, которые взаимосвязаны и, в известной степени, взаимообусловлены:
1) гетерометрический (механизм Франка-Старлинга);
2) гомеометрический механизм;
3) усиление симпатоадреналовых влияний на миокард;
5) активация ренин-ангиотензиновой системы.
Включение компенсаторных механизмов ведет к (1) увеличению ударного объема сердца, (2) повышению МОС, (3) тоногенной дилятации, (4) гипертрофии миокарда.
Рост ударного (систолического) объема сердца происходит за счет гетерометрического и гомеометрического механизмов усиления сокращения сердца. Первый из них обеспечивается законом Франка-Старлинга – чем интенсивнее растягивается миокард повышенным объемом крови (увеличение диастолического наполнения и конечнодиастолического объема), тем с большей силой сокращаются предварительно растянутые волокна миокарда. Однако если степень растяжения кардиомиоцитов превышает допустимые пределы (более 20-25% исходного уровня), то сила сокращения сердца снижается.
Расширение полостей сердца, сопровождаемое увеличением ударного объема сердца, называется тоногенной дилятацией. Тоногенная дилятация считается наиболее благоприятным приспособительным механизмом сердца, т.к. для поддержания адекватного МОС не требуется повышения частоты сокращения сердца. Поэтому динамика сердечного цикла практически не меняется, а усиленная систола способствует выбросу большего количества крови из желудочков и меньшему остаточному объему.
Сердечный цикл состоит из систолы и диастолы, и при 75 сокращений сердца в минуту на систолу приходится 0,33, на диастолу – 0,47 сек. Наиболее энергоемкой фазой систолы является изометрическое напряжение, которое по времени занимает 0,03 сек. в цикле. Если частота сокращения сердца не изменяется, то на эту фазу приходится не более 2,3 сек. за одну минуту, а на восстановление энергетических ресурсов миокарда – около 36 секунд. Когда частота сокращений сердца повышается, то возрастает общая продолжительность энергоемкой фазы (например, при тахикардии в 100 ударов она достигает уже 3 секунд на протяжении одной минуты), а время на восстановление энергоресурсов укорачивается до 27 вместо 36 секунд в минуту.
В восстановительный период происходит ресинтез, в первую очередь, белков и других органических компонентов, в том числе высокоэргических фосфорных соединений, нормализация электролитного состава кардиомиоцитов. Укорочение восстановительного периода приводит к нарушению этих процессов. Наконец, ограничение длительности диастолической фазы при тахикардии ухудшает гемодинамические характеристики сердца: во время диастолы желудочки не успевают заполняться кровью, и систола становится менее полноценной.
Длительная нагрузка на сердце вызывает развитие специфических обменных и структурных изменений, выражающихся в повышении массы и работоспособности кардиомиоцитов – гипертрофия миокарда. Нарастающая по интенсивности нагрузка – систолическое и диастолическое перенапряжение, активирует генетический аппарат сердца (протоонкогены c-fos, c-myc) и приводит к усиленному синтезу белков и увеличению массы и объема кардиомиоцитов. Не исключается, что протоонкогенез стимулируется катехоламинами и локально образующимся в миокарде ангиотензином-II. Спустя 1-2 недели интенсивной работы сердца развивается гипертрофия миокарда, т.е. увеличивается объем каждого мышечного волокна. Хотя общее количество кардиомиоцитов остается без изменений, масса каждого волокна прогрессивно увеличивается, в связи с чем общая масса миокарда возрастает в 1,5-3 раза. Гипертрофия миокарда снижает нагрузку на единицу мышечной массы до нормального уровня.
Гипертрофированное сердце отличается от нормального рядом обменных, функциональных и структурных признаков, которые позволяют ему длительное время преодолевать повышенную нагрузку при сердечной недостаточности. Вместе с тем, они создают предпосылки для возникновения в кардиомиоцитах патологических изменений, которые выражаются, во-первых, в нарушении нервной регуляции гипертрофированного миокарда (в связи с отставанием роста нервных окончаний от темпов увеличения массы кардиомиоцитов); во-вторых, в ограничении сосудистого обеспечения миокарда (в связи с отставанием роста артериол и капилляров от увеличения массы кардиомиоцитов – т.е. развивается относительная коронарная недостаточность); в-третьих, в снижении энергообеспечения кардиомиоцитов (в связи с ограничением числа митохондрий каждого кардиомиоцита на единицу его массы); в-четвертых, в падении сократительной функции сердца (в связи с изменением соотношения между легкими, т.е. длительно живущими, и тяжелыми, т.е. коротко живущими цепями головок миозина, являющимися носителями АТФ-азной активности); в-пятых, в изменении пластических процессов в кардиомиоцитах – вследствие снижения числа митохондрий нарушаются метаболизм, объем микроциркуляции, уменьшаются функциональные резервы сердца.
Дистрофические изменения сердечной мышцы, в конечном счете, ведут к ослаблению миокарда и расширению камер сердца – миогенной дилятации. Ослабление миокарда повышает конечнодиастолическое давление крови в полостях предсердий, что вызывает раздражение барорецепторов устья полых вен, области синоатриального узла и последующую тахикардию, которая является энергетически неблагоприятным механизмом компенсации сердечной недостаточности из-за нарушений обменных и гемодинамических показателей.
В динамике компенсаторной гипертрофии миокарда Ф.З. Меерсон выделяет три основных стадии: (1) аварийную, (2) завершившейся гипертрофии и относительно устойчивой гиперфункции миокарда, (3) постепенного истощения, изнашивания и прогрессирующего кардиосклероза.
Аварийная стадия развивается непосредственно после повышения нагрузки на сердце. Она характеризуется сочетанием патологических изменений в миокарде (нарушений энергетического обмена, снижение уровня АТФ, креатинфосфата, дисбаланса ионов, истощения гликогена и т.п.) с мобилизацией резервов его миокарда. Нагрузка на единицу массы возрастает, а гипертрофия наступает в течение 10-12 дней. Масса сердца увеличивается в 1,5-3 раза за счет усиленного синтеза белков и нуклеопротеидов, энергообеспечивающих структур и утолщения кардиомиоцитов. Правда, масса различных структур растет гетеросинхронно – раньше энергообеспечивающих, затем сократительных и остальных структур.
Стадия завершившейся гипертрофии и относительно устойчивой функции миокарда. Процесс гипертрофии миокарда завершился, и его масса увеличилась. Патологические проявления в миокарде исчезли, нормализовались метаболические, гемодинамические и другие его показатели. Гипертрофированное сердце приспособилось к новым условиям нагрузки и в течение длительного времени полностью ее компенсирует.
Стадия постепенного истощения и прогрессирующего кардиосклероза характеризуется снижением скорости образования РНК и синтеза белка, что ведет к развитию кардиосклероза. Нарушается энергетическое, метаболическое, сосудистое, регуляторное обеспечение миокарда. Все выше перечисленное через 1,5 года ведет к возникновению хронической недостаточности сердца и далее к недостаточности кровообращения.
Таким образом, снижение сократительной функции сердца является итогом сердечной недостаточности различной этиологии. Этот факт дает основание для заключения: несмотря на различие причин и известное своеобразие начальных звеньев патогенеза сердечной недостаточности, ее конечные звенья – на клеточном и молекулярном уровнях едины. Среди них в качестве главных выделяют следующие:
1. Нарушение энергообеспечения кардиомиоцитов;
2. Повреждение мембранного аппарата и ферментов кардиомиоцитов;
3. Дисбаланс ионов и жидкости в кардиомиоцитах;
4. Расстройство механизмов нейрогуморальной регуляции сердца.
Экстракардиальные механизмы компенсации сердечной недостаточности.Помимо (интра)кардиальных механизмов компенсации – (1) увеличения ударного объема, (2) тахикардии, (3) тоногенной дилятации и (4) гипертрофии миокарда, существуют экстракардиальные компенсаторные механизмы (таблица 3).
Самым ранним и наиболее существенным механизмом компенсации нарушенной насосной функции сердца является (1) повышение активности симпатоадреналовой, далее (2) ренин-ангиотензин-альдостероновой систем, активация синтеза (3) предсердного натрийуретического гормона, (4) дигиталисоподобного фактора, (5) эндотелинов и (6) вазопрессина (данные таблицы 3). Кроме вышеперечисленных, сюда же относят изменения в дыхательной, сосудистой системах, а также в системе крови.
К компенсаторным механизмам, связанным с функцией дыхательной системы, относят (1) одышку, (2) гиперпноэ, (3) совершенствование корреляций между альвеолярной вентиляцией и перфузией легких, (4) повышение диффузионной поверхности легких, (5) увеличение массы дыхательных мышц.
К компенсаторным механизмам, связанным с функциями кровообращения и системы крови, относят: (1) перераспределение сосудистого тонуса, (2) централизацию кровообращения, или улучшение кровоснабжения жизненно важных органов, (3) увеличение массы циркулирующей крови за счет ее выхода из депо, (4) повышение кислородной емкости крови за счет выхода эритроцитов из костного мозга вследствие стимуляции эритропоэза, (5) сдвиги кривой диссоциации оксигемоглобина вправо и влево, соответственно, в верхней и нижней частях ее инфлексии, (6) нарастание коэффициента утилизации кислорода тканями (КУО = А-В/А 100, или 200-140/200×100 = 30%, где А и В – содержание кислорода в артериальной и венозной крови).
Основные экстракардиальные механизмы компенсации
Использованные источники:
Аритмия сердца. Сердечная недостаточность

Аритмия сердца – это нарушения периодичности возбуждения и сокращения сердца, его ритмичности.
Аритмия, болезнь широко распространённая, она может возникнуть во время любого сердечного заболевания и под воздействием вегетативного, эндокринного и прочих метаболических нарушений. Серьёзное значение имеют электролитные расстройства, а именно, отклонения от нормы калия и кальция, содержащихся в клетке. Аритмия может возникнуть при интоксикации организма и при некоторых действиях лекарства, она может быть связана с врождёнными особенностями проводящей системы.
В основе аритмии лежит нарушение электрофизиологических качеств проводящей системы и сократительного миокарда. Диагностируют аритмии, как правило, по ЭКГ, в виде: синусовой аритмии, пароксизмальной тахикардии, экстрасистолии, трепетания предсердий, мерцания предсердий, трепетания и мерцания желудочков, атриовентрикулярной блокады, синоатриальной блокады, блокады ножек пучка Гисса и т.д.
Сердечная недостаточность
Это недостаточность кровообращения. Хронической сердечной недостаточностью называют состояние, при котором сердце не может справиться со своими насосными функциями, то есть, оно не обеспечивает нормального кровообращения. Причин появлению такого состояния довольно много: это и ишемическая болезнь сердца, и его пороки, и артериальная гипертензия, а также диффузные заболевания лёгких, дистрофия миокарда, миокардит и пр.
Симптомы и течение хронической сердечной недостаточности.
Симптомы различают в зависимости от поражённого отдела сердца. Так, при недостаточности работы левого желудочка у больного появляется одышка, при сидении наблюдается упор рук в колени, в целом сердцебиение учащенное. Параллельно может наблюдаться проявление недостаточности мозгового кровообращения – головокружения, потемнение в глазах и даже обмороки. Недостаточность работы правого желудочка сердца проявляется в набухании вен шеи, синюшностью кончиков пальцев, губ и носа, увеличением печени, различными отёками тела и полостей организма. При длительном течении сердечной недостаточности кожа больного становится тонкой, дряблой, она блестит, отёки покрывают все тело, происходит постепенное истощение организма.
Нормальный ритм сердцебиения обеспечивается автоматически синусовым узлом, он так и называется — синусовый. Частота синусового ритма у большинства взрослых здоровых людей, находящихся в состоянии покоя, составляет 60-75 ударов в минуту.
Синусовая аритмия
Синусовая аритмия – это синусовый ритм, при котором превышена разница между интервалами R-R на ЭКГ на 0,1 с. Дыхательная синусовая аритмия – это физиологичное явление, которое более заметно у молодых людей и при медленном глубоком дыхании по пульсу или ЭКГ. Среди факторов, учащающих синусовый ритм, можно отметить физические и эмоциональные нагрузки, симпатомиметики. Они способны уменьшить или полностью устранить дыхательную синусовую аритмию. Синусовая аритмия, которая не связанна с дыханием, встречается крайне редко. Сама по себе она лечения не требует.
Синусовая тахикардия
Временные проявления синусовой тахикардии возникают под влиянием симпатомиметиков, атропина, при быстром снижении артериального давления любого происхождения, после приёма алкогольных напитков. Стойкая синусовая тахикардия возникает во время лихорадки, тиреотоксикоза, миокардита, при сердечной недостаточности, проявлении анемии и тромбоэмболии легочной артерии. Она может сопровождаться ощущением собственного сердцебиения.
Лечение аритмии и сердечной недостаточности должно быть направлено на устранение основного заболевания. При проявлении тахикардии, которая обусловлена тиреотоксикозом, вспомогательное значение имеет использование бета-адреноблокаторов. Синусовая тахикардия, связанная с нейроциркуляторной дистонией, лечится применением в малых дозах седативных средств и бета-адреноблокаторами. При тахикардии, обусловленной сердечной недостаточностью, врач назначает сердечные гликозиды.
Использованные источники:
