Перегрузочная форма сердечной недостаточности патогенез
Патогенез перегрузочной сердечной недостаточности при увеличении постнагрузки.
Постнагрузка – сопротивление изгнанию крови из желудочков в аорту и легочную артерию.Основной фактор, определяющий постнагрузку – общее периферическое сопротивление сосудов (ОПСС).При увеличении ОПСС возрастает и постнагрузка. Другими словами – увеличение постнагрузки – это появление дополнительного препятствия при изгнании крови из желудочков. Таким препятствием могут быть артериальные гипертензии, стеноз клапана аорты, сужение устья аорты и легочной артерии, гидроперикард.
Увеличение преднагрузки называют перегрузкой давлением.
Патогенез сердечной недостаточности
В условиях перегрузки давлением
(на примере стеноза клапана аорты):
Стеноз клапана аорты как дополнительное препятствие
для изгнания крови из левого желудочка в аорту.
Удлинение систолы с целью увеличения времени контакта актина и миозина кардиомиоцитов.
1. Увеличение внутримиокардиального
напряжения во время систолы.
2. Увеличение силы сокращения сердечной мышцы.
3. Укорочение диастолы.
Ишемизация сердечной мышцы.
Нарушение энергообеспечения миокарда
1. Повреждение мембран и ферментных систем кардиомиоцитов
2. Дисбаланс ионов и жидкости в кардиомиоцитах
3. Расстройства нейро-гуморальной регуляции сердца
Снижение напряжения кардиомиоцитов в частности
и миокарда в целом при сокращении.
Снижение силы и скорости сокращений и раслаблений миокарда
Уменьшение ударного объема УО и минутного объема сердца МОС.
Нарушения гемодинамики с явлениями ишемизации в одних регионах
и застоя крови в других.
Явления недостаточности по органам и системам.
Примечание: курсивом выделен фрагмент патогенеза сердечной недостаточности, общий для всех форм СН различного генеза.
Нарушения гемодинамики
При острой левожелудочковой недостаточности
Нарушения гемодинамики
При хронической левожелудочковой недостаточности
Наблюдается ишемизация органов и тканей по большому и по малому кругам кровообращения
Ишемизация по большому кругу
Ишемизация по малому кругу
Нарушения гемодинамики
При острой правожелудочковой недостаточности
При хронической правожелудочковой недостаточности
Застой в венозной системе большого круга
Отеки периферических тканей, в т. ч. печени
Увеличение давления в печени, сдавление питающих артерий,
нарушение питания клеток печени
Разрастание соединительной ткани
Кардиогенный цирроз печени,
Общие нарушения гемодинамики при СН
(независимо от локализации)
1. Уменьшение МОК: причина – снижение сократительной функции сердца.
2. Увеличение систолического объема в результате неполной систолы:
= сопротивление для оттока;
= прямое повреждение миокарда.
3. Увеличение конечного диастолического давления в желудочках сердца: в результате увеличения количества крови, остающегося в желудочках после систолы + нарушение расслабления миокарда.
4. Дилатация полостей сердца: в результате увеличения конечного диастолического объема и растяжения миокарда.
5. Увеличение давления крови в венах и полостях сердца:
= при ЛЖН – в левом желудочке и легочных венах;
= при ПЖН – в правом предсердии и vv.cavae.
6. Снижение скорости сократительного процесса: это увеличиваетпериод изометрического напряжения и систолы в целом.
Кардиальные механизмы
Компенсации сердечной деятельности
Условно выделяют 4 (четыре) кардиальных механизма сердечной деятельности при СН.
1. Гетерометрический механизм компенсации Франка-Старлинга:
Если степень растяжения мышечных волокон превышает допустимые границы, то сила сокращения снижается.
При допустимых перегрузках линейные размеры сердца увеличиваются не более, чем на 15-20%. Такое расширение полостей называется тоногенной дилатацией и сопровождается увеличением УО.
Дистрофические изменения в миокарде ведут к расширению полостей без увеличения УО. Это – миогенная дилатация (признак декомпенсации).
2. Изометрический механизм компенсации:
Изометрический механизм более энергоемкий, чем гетерометрический.
Гетерометрический механизм энергетически более выгоден, чем изометрический. Поэтому клапанная недостаточность протекает более благоприятно, чем стеноз.
3. Тахикардия: возникает в ситуациях:
= Увеличение давления в полых венах.
= Увеличение давления в правом предсердии и растяжение его.
= Изменение нервных влияний.
= Изменение гуморальных экстракардиальных влияний.
Тахикардия – энергетически невыгодный механизм компенсации. Причины: = Повышение потребности миокарда в кислороде.
= Укорочение диастолы → уменьшение периода отдыха миокарда.
= Укорочение диастолы → желудочек не успевает заполниться кровью.
= Неполное заполнение кровью желудочков делает невозможным реализацию гетерометрического механизма компенсации.
= Менее полноценная систолы.
4. Усиление симпатоадреналовых влияний на миокард: включается при снижении УО и значительно усиливает силу сокращений миокарда.
Гиперфункция миокарда.
Причины, виды, патогенетическая значимость.
Кардиальные механизмы компенсации увеличивают интенсивность работы сердца. Увеличение интенсивности работы сердца называется гиперфункцией миокарда.
Патогенетическая значимость гиперфункции – это универсальный механизм декомпенсации.
М.б. гиперфункция: а) изометрическая (перегрузка давлением);
б) изотоническая (перегрузка объемом).
Гипертрофия миокарда
Гипертрофия – это увеличение объема и массы миокарда. Возникает при реализации кардиальных механизмов компенсации. Кардиальные механизмы компенсации увеличивают интенсивность работы миокарда на фоне повышенного синтеза белков и нуклеиновых кислот. Поэтому объем и масса миокарда увеличивается.
Биологическая значимость и особенности компенсированной гипертрофии:
1. При повышенной нагрузке орган выполняет необходимую работу за счет возросшей массы.
2. Гипертрофированный миокард имеет морфофункциональные особенности, в которых заложены возможности и предпосылки для дальнейшей декомпенсации:
= Рост нервных волокон отстает от скорости увеличения массы кардиомиоцитов → в условиях повышенной нагрузки возможен дефицит нервных влияний на миокард.
= Рост артерий и капилляров отстает от роста кардиомиоцитов.
= Уменьшение клеточной поверхности на единицу массы клетки → ионный дисбаланс.
= Рост митохондрий отстает от роста кардиомиоцитов → дефицит энергии.
= нарушение кардиомиоцитарных пластических процессов вследствие вышеперечисленных причин.
Аварийная стадия – сразу после повышения нагрузки. Характерено:
1. Повышенный синтез белков и утолщение мышечных волокон.
2. Мобилизация гликогена и исчезновение его глыбок из цитоплазмы кардиомиоцитов.
3. Уменьшение содержания креатинфосфата.
4. Дисбаланс ионов (K ↓, Na ↑).
5. Накопление лактата.
Стадия завершившейся гипертрофии – масса и объем миокарда увеличены. Миокард полностью справляется с обычной и повышенной нагрузкой. Потребление О2 и образование энергии сбалансировано. Нарушения гемодинамики нормализованы.
НО! Если повышенная нагрузка на сердце действует длительное время или появилось дополнительное повреждение миокарда, то гипертрофия переходит в 3-ю стадию.
Использованные источники:
4.Перегрузочная форма сердечной недостаточности, этиология и особенности механизмов развития. Механизмы компенсации.
Перегрузочная форма сердечной недостаточности возник.в результ.чрезмерной нагрузки на сердце.
Существуют варианты в зависимости от того, что страдает:
а) Перегрузочная СН при увеличении преднагрузки.
Преднагрузка – объем крови, притекающий к сердцу. ↑ преднагрузки при гиперволемии, полицитемии, гемоконцентрации, недостаточность клапанов. ↑ преднагрузки(перегрузка объемом) – это увеличении объема перекачиваемой крови.
Патогенез( недостат.клапана сердца аорты): при систоле часть крови возвращается в левый желудочек =>↓диастолич.давления в аорте => кровоснабжение миокарда только в диастолу => ↓ кровенаполнения миокарда и его ишемизация => ↓ сократимости миокарда => развитие СН.
б) Перегрузочная СН при увеличении постнагрузки.
Перегрузка – сопротивление изгнанию крови из желудочков в аорту и легочную артерию. Фактор посленагрузки – ОПСС. При ↑ ОППС -↑ посленагрузка. ↑ постнагрузки – это препятствие при изгнании крови. Таким препятствием может быть артериальная гипертензия, стеноз клапана аорты, сужение аорты и легочной артерии.
Увеличение преднагрузки называют перегрузкой давлением.
Патогенез(стеноз клапана аорты): при систоле сердце прикладывает больше силы для того, чтобы протолкнуть порцию крови через суженное отверстие в аорту => за счет удлинения систолы и укорочения диастолы => кровоснабжение миокарда только в диастолу => ↓ кровенаполнения миокарда и ишемизация миокарда => ↓ сократимости миокарда => на молекулярном и клеточном уровне механизмы патогенеза СН при самых различных причинах и формах СН => нарушение энергообеспечения миокарда => повреждение мембран и ферментных систем кардиомиоцитов => дисбаланс ионов и жидкости в кардиомиоцитах =>расстройства нейро-гуморальной регуляции сердца => ↓ силы и скорости сокращений и расслаблений миокарда => развитие СН.
Компенсированная и декомпенсированная сердечная недостаточность.
Компенсированная СН – состояние, когда поврежденное сердце обеспечивает органы и ткани адекватным кол-ом крови при нагрузке и в покое за счет реализации кардиальных и экстракардиальных механизмов компенсации.
Декомпенсированная СН – состояние, когда поврежденное сердце не обеспечивает органы и ткани адекватным кол-ом крови несмотря на использование механизмов компенсации.
1.Основные этапы становления патофизиологии. Роль отечественных (В.В.Патушев, А.А.Богомолец, И.И.Павлов, И.М.Сеченов, И.Р.Петров, А.М.Чернух, Г.И.Крыжановский) и зарубежных (Р.Вирхов, Ю.Конгейм, Г.Шаде, Г.Селье) ученных.
Первый период(1542-1863)-преподавание пат.физа,ее отдельных эл.вместе с анатомией, физиологией,терапией в основном клинцистами.Впервые применил термин патофизиология Галлиот в 1819г.
Второй период (1863-1924 гг.). Выделением преподавания физиологии и патофизиологии в самостоятельные дисциплины.
Третий период (1924-1950 гг.). В 1924 г.по предложению акад. А.А.Богомольца и проф. С.С.Халатова кафедры общей патологии университетов были переименованы в кафедры пат.физа. Бурное развитием П.Ф.и формированием научных школ, созданием исследовательских институтов.
Четвертый период (с 1950 г. и по настоящее время). Объединению патофизиологов во Всесоюзное общество патофизиологов. С 1957 г. В 1970 г. в Баку прошел I Всесоюзный съезд патофизиологов, а в 1972 г. в Ростове-на-Дону — I международный конгресс патофизиологов. В 1991 г. организуется Международное общество патофизиологов. В результате патофизиология становится наукой, признанной на международном уровне.
Патофизиология — наука, изучающая жизнедеятельность больного организма. Иначе: основные закономерности возникновения, механизма развития (патогенеза) и исхода болезни (выздоровление, реабилитация или смерть).
Задачи патофизиологии:Изучение наиболее общих (типичных) закономерностей отклонений от нормального течения работы клеток и организма в целом. Пашутин- преобразовал общую патологи ю в науку экспериментальную, яв. Автором крупного 1 руководства по патфизу. Богомолец- указал на роль соед ткани в регуляции функций клеток, разделил тк и орг, доказал значение в формировании противоинфекционной и противораковой резистентности орг, разработал антиретикулоэндотелиальную цитотоксическую сыворотку(стимул.функцию соед тк и ↑ резистентность). Петров- изуч.патогенез шока – травматического, ожогового, электрического постгеморрагического, анафил,разработал способы патогенетич.терапии и профилактики шока. Чернух – учение о нейрососудистой регуляции жизнедеятельности клетки при различных пат.процессах вообще и воспалении в частности. Крыжановский-создателем теории генераторных механизмов нейропатологических СД, характеризующихся гиперактивностью систем, основоположник учения о детерминанте. Вирхов— основатель теории клеточной патологии- рассматривает клетку как материальный субстрат болезни, а саму болезнь — как определенную сумму поражений множества отдельных клеток. Конгейм — проследил все стадии воспалит.процесса и описал выхождение лейкоцитов через стенки сосуда как активный процесс эмиграции, их превращение в гнойные шарики и участие в процессе восстановления тканей. Шаде— охарактеризовал типичные физико-химические сдвиги в очагах воспаления: местный ацидоз, гиперосмолярность, накопление ионов калия в интерстициальной жидкости, увеличение тканевого гидростатического давления. Селье— гипотеза общего адаптационного синдрома,
2. Ожирение, виды, этиология, патогенез, последствия. Ожирение – избыточное отложение жира в жировой ткани. Избыток лептина подавляет действие инсулина на клетки печени(инсулин активирует адипоциты,↑ образование лептина, а он воздействует на собственные рецепторы, локализованные на поверхности бета кл, тормозит секрецию инсулина). Первичное ожирение наруш.гормон.связи между жировой тканью и гипоталамусом. Генетическое заболевание, главная черта-абсолютная или относительная лептиновая недостаточность. Вторичное ожирение-сд, нарушение соотношения между липолиза и липогенеза, симптоматический характер и с расстройствами(эндокринопатии, опухоли мозга, нарушения мозгового кровообращения). Степени ожирения – 1ст (масса тела увел на 30%) 2 ст( на 30-50%), 3ст(более чем на 50%).Гипертрофическое ожирение— ↑ размеров адипоцитов. Гиперпластическое ожирение-↑ кол-ва адипоцитов.
По этиологии: экзогенно-конституциональное(переедание), гипоталамическое ожирение(поражения гипоталамуса(травмы гол мозга,опухоли мозга), гормональное ожирение(гипо-, гиперфункцией желез внутренней секреции).По патогенезу: алиментарное(чрезмерном потреблении пищи); метаболическое(↑синтезом жира из углеводов); энергетическое(недостаточное использование жиров в качестве источника энергии).
Последствия: ↓ур. общего белка крови за счет ↓ концентр альбуминов, ↑ фибриногена, продуктов деградации фибрина,↓ ур.гепарина=> наруш.транспорта липидов,↓ фибринолитической активности и ↑ тромбогенных свойств крови=>тромбоэмболий. Возникают нарушения функций ЦНС: утомляемость, сонливость, ухудшение памяти;преждевременное старение, изменения во внутр.органах(жировая инфильтрация печени).
Использованные источники:
Сердечная недостаточность: понятие, формы
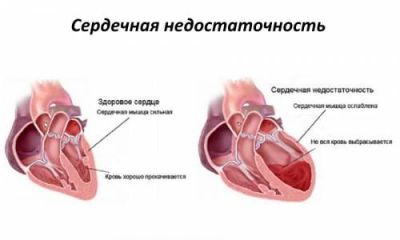
Сердечная недостаточность (СН)—типовая форма патологии сердечно-сосудистой системы, характеризующаяся тем, что насосная функция сердца не обеспечивает адекватный метаболическим потребностям организма уровень системной гемодинамики [некомпенсированная форма СН] или поддерживает его благодаря реализации предсуществующих и/или вновь формируемых компенсаторных механизмов организма [компенсированная форма СН].
Формы сердечной недостаточности
Ниже приведены основные формы сердечной недостаточности:
а) острая (минуты, часы);
б) хроническая (недели, месяцы, годы).
Б. По степени выраженности:
B. По патогенезу:
в) смешанная (комбинированная — сочетание миокардиальной и перегрузочной).
Г. По первично-нарушенной фазе сердечного цикла:
Д. По локализации:
а) левожелудочковая, для которой характерны уменьшение выброса крови в аорту, перерастяжение левого сердца и застой крови в малом круге кровообращения;
б) правожелудочковая, для которой характерны уменьшение выброса крови в малый круг кровообращения, перерастяжение правого сердца и застой крови в большом круге кровообращения;
в) тотальная (сочетание лево- и правожелудочковой недостаточности). Дифференциация форм сердечной недостаточности по механизму ее развития наиболее значима для практикующего врача, т.к. позволяет ему сориентироваться в ответе на главный вопрос: «кто виноват в нарушении насосной функции сердца»? Такими «виновниками» могут быть патогенетически значимые изменения: 1) контрактильных свойств миокарда; 2) пред-нагрузки (значительное поступление крови в полости сердце); 3) постнагрузки (снижение оттока крови из полостей сердца).
Миокардиальная форма сердечной недостаточности
Миокардиальная форма сердечной недостаточности возникает при повреждении миокарда в условиях развития ИБС, миокардитов, миокардиодистрофий, кардиомиопатий. Патогенетическую основу данной формы составляют патогенетически значимые изменения одного из двух основных свойств миокарда — сократимости (силы и скорости сокращения кардиомиоцитов) и расслабляемо-сти (скорости и глубины расслабления мышечных волокон после их сокращения).
Перегрузочная форма сердечной недостаточности
Перегрузочная форма сердечной недостаточности развивается в условиях перегрузки сердца:
а) объемом (при пороках сердца с недостаточностью клапанов, врожденном незаращении межжелудочковой перегородки, гиперволемии)
б) сопротивлением (при пороках сердца со стенозами отверстий, коарктации аорты, артериальной гипертензии, полицитемии).
Диастолическая сердечная недостаточность
Установлено, что диастолическая сердечная недостаточность всегда включает диастолическую дисфункцию, но ее наличие еще не свидетельствует о сердечной недостаточности. Диастолическую сердечную недостаточность диагностируют значительно реже, чем диастолическую дисфункцию, и наблюдают не более чем у 1/3 больных ХСН.
Выделяют 3 ступени перехода от диастолической дисфункции к диастолической сердечной недостаточности. На 1-й ступени под влиянием различных повреждающих агентов (перегрузок, ишемии, инфаркта. гипертрофии левого желудочка и т.д.) нарушается процесс активного расслабления миокарда и раннего наполнения левого желудочка, что на этом этапе полностью компенсируется активностью левого предсердия, поэтому не проявляется даже при нагрузках. Прогрессирование заболевания и повышение жесткости камеры ЛЖ сопровождается вынужденным ростом давления заполнения ЛЖ (предсердие уже не справляется!), особенно заметным при нагрузках. Наблюдают еще большее затруднение притока крови к левому желудочку и патологический рост давления в легочной артерии, что снижает толерантность к нагрузкам (2-я ступень). Дальнейший рост давления заполнения ЛЖ (3-я ступень) полностью «выводит из строя» левое предсердие; приток крови к желудочку (отток крови из легких) снижен критически, что сопровождается падением сердечного выброса, резким снижением толерантности и застоем в легких, т. е. формированием развернутой картины ХСН.
Таким образом, переход от диастолической дисфункции левого желудочка к диастолической сердечной недостаточности обусловлен классическим вариантом развития застоя, вызванного уменьшением оттока крови из легких, ухудшением активного расслабления миокарда и повышением жесткости камеры ЛЖ. Ключом к решению проблемы считают улучшение активного расслабления и увеличение податливости камеры левого желудочка.
Другой особенностью диастолической сердечной недостаточности по сравнению с традиционным (классическим) вариантом ее развития является относительно лучший прогноз — уровень годичной летальности при диастолическом варианте примерно в два раза меньше, чем при «классической» систолической хронической сердечной недостаточности. Однако специалисты считают, что такое «благополучие» обманчиво, поскольку смертность от систолической ХСН постоянно снижается, а от диастолической сердечной недостаточности — из года в год остается на одном уровне,что можно объяснить отсутствием достаточно эффективных средств лечения больных с диастолической формой хронической сердечной недостаточности.
При ухудшении насосной функции желудочков сердца увеличение пред-нагрузки способно поддерживать сердечный выброс. В результате этого на протяжении длительного времени происходит ремоделирование левого желудочка: он становится более эллиптоидным, расширяется и гипертрофируется.
Будучи изначально компенсаторными, эти изменения в конечном счете увеличивают диастолическую ригидность и напряженность стенки (миокардиальный стресс), нарушая работу сердца, особенно во время физической нагрузки. Увеличенное напряжение сердечной стенки повышает потребность в кислороде и ускоряет апоптоз (запрограммированная клеточная гибель) миокардиальных клеток.
Использованные источники:
Сердечная недостаточность, ее виды. Этиология и патогенез.
Виды сердечной недостаточности по происхождению
• Миокардиальная форма развивается преимущественно в результате непосредственного повреждения миокарда.
• Перегрузочная форма сердечной недостаточности возникает преимущественно в результате перегрузки сердца (увеличения пред- или постнагрузки).
• Смешанная форма сердечной недостаточности — результат сочетания прямого повреждения миокарда и его перегрузки.
по скорости развития
• Острая (развивается за несколько минут и часов). Является результатом инфаркта миокарда, острой недостаточности митрального и аортального клапанов, разрыва стенок левого желудочка.
• Хроническая (формируется постепенно, в течение недель, месяцев, годами). Является следствием артериальной гипертензии, хронической дыхательной недостаточности, длительной анемии, пороков сердца. Течение хронической сердечной недостаточности может осложнять острая сердечная недостаточность.
по первичности механизма развития
• Первичная (кардиогенная). Развивается в результате преимущественного снижения сократительной функции сердца при близкой к нормальной величине притока венозной крови к нему.
• Вторичная (некардиогенная). Возникает вследствие первичного преимущественного уменьшения венозного притока к сердцу при близкой к нормальной величине сократительной функции миокарда.
Самыми распространенными причинами сердечной недостаточности являются артериальная гипертензия.
Сердечная недостаточность может быть вызвана тремя причинами:
Первая — из-за чрезмерной перегрузки сердца, вызванной повышенным объёмом циркулирующей крови и/или высоким давлением. Подобное состояние может быть вызвано, например при гипертонической болезни сердца, приобретённых или врождённых пороках сердца, лёгочном сердце и так далее.
Вторая причина— снижение сократительной (насосной) функции сердечной мышцы и уменьшением массы миокарда. Данная ситуация возникает например в следствии постинфарктного кардиосклероза, инфаркта миокарда, аневризмы сердечной мышцы и прочее.
И третья — дегенеративные изменения миокарда, которые возникают в следствии развития гемохроматоза, амилоидоза и других патологических процессов.
Также, причинами сердечной недостаточности могут быть кардиомиопатия, миокардит, миокардиодистрофии самой разной этиологии и отравления кардиотропными ядами, последнее свойственно острой форме сердечной недостаточности.
Патогенез синдрома сердечной недостаточности напрямую зависит от причин. Чаще всего ведущее значение оказывает понижение сократимости миокарда, как правило обусловленное сбоём энергетического обеспечения функции миокарда из-за низкой эффективности использования и недостаточного образования АТФ в мышце сердца.
Способствовать этому могут:
-Недостаточное поступление кислорода в миокард при гипоксемии у пациентов с дыхательной недостаточностью, пониженном кровотоке в сосудах мышцы сердца, анемии и так далее;
— Перегрузка миокарда при гиперфункции сердечной мышцы, тиреотоксикозе, артериальной гипертензии и других заболеваниях;
— Неполная утилизация продуктов и кислорода в миокарде по причине нехватки некоторых ферментов, например при авитаминозе В, сахарном диабете и так далее.
Большое значение в патогенезе сердечной недостаточности играет нарушение функциональных способностей клеточных мембран, которые возникают при различных формах дистрофии сердечной мышцы, приводящие к нарушению потоков катионов кальция, натрия и калия в фазы диастолы и систолы, что в итоге приводит к значительному снижению сократительной силы миокарда.
Ишемическая болезнь сердца. Причины и механизмы развития. Инфаркт миокарда.
Ишемическая болезнь сердца (сокращенно ИБС) — это болезнь, объединяющая стенокардию, инфаркт миокарда и атеросклеротический кардиосклероз. ИБС развивается из-за недостаточного кровоснабжения коронарных артерий сердца вследствие сужения их просвета.
Причины и механизм развития
Несмотря на то, что сердце в организме перекачивает кровь, оно само нуждается в кровоснабжении. Сердечная мышца (миокард) получает кровь по двум артериям, которые отходят от корня аорты и носят название коронарных (из-за того, что они огибают сердце как будто короной). Далее эти артерии разделяются на несколько более мелких ветвей, каждая из которых питает свой участок сердца.
Больше артерий, приносящих кровь к сердцу, нет. Поэтому при сужении просвета или закупорке одной из них, участок сердечной мышцы испытывает недостаток кислорода и питательных веществ, развивается болезнь.
Основной причиной ИБС в настоящее время считается атеросклероз коронарных артерий с отложением в них холестериновых бляшек и сужением просвета артерии (коронарная болезнь). В результате кровь не может в достаточном объеме поступать к сердцу.
Поначалу недостаток кислорода проявляется только во время повышенной нагрузки, например при беге или быстрой ходьбе с грузом. Появляющиеся при этом боли за грудиной носят название стенокардии напряжения. По мере сужения просвета коронарных артерий и ухудшения метаболизма сердечной мышцы боли начинают появляться при все более низкой нагрузке, а в конце концов и в покое.
Одновременно со стенокардией напряжения может развиваться хроническая сердечная недостаточность, проявляющаяся отеками и одышкой.
При внезапном разрыве бляшки может наступить полное перекрытие просвета артерии, инфаркт миокарда, остановка сердца и смерть. Степень поражения сердечной мышцы при этом зависит от того, в какой артерии или разветвлении произошла закупорка – чем крупнее артерия, тем хуже последствия.
Для того чтобы развился инфаркт миокарда, просвет артерии должен уменьшиться не менее чем на 75%. Чем медленнее и постепеннее это происходит, тем сердцу легче приспособиться. Резкая закупорка наиболее опасна и часто ведет к смерти
Инфаркт миокарда — это тяжелое заболевание, характеризующееся гибелью части сократительных клеток миокарда с последующим замещением погибших (некротизированных) клеток грубой соединительной тканью (т.е. формированием постинфарктного рубца).
Механизм инфаркта миокарда — разрыв атеросклеротической бляшки, часто при умеренном стенозе до 70% в коронарной артерии. При этом коллагеновые волокна обнажаются, происходит активация тромбоцитов, запускается каскад реакций свертывания, что приводит к острой окклюзии коронарной артерии. Если восстановления перфузии не происходит, то развиваются некроз миокарда (начиная с субэндокардиальных отделов), дисфункция пораженного желудочка (в подавляющем большинстве случаев — левого), аритмии.

Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.
Использованные источники:
